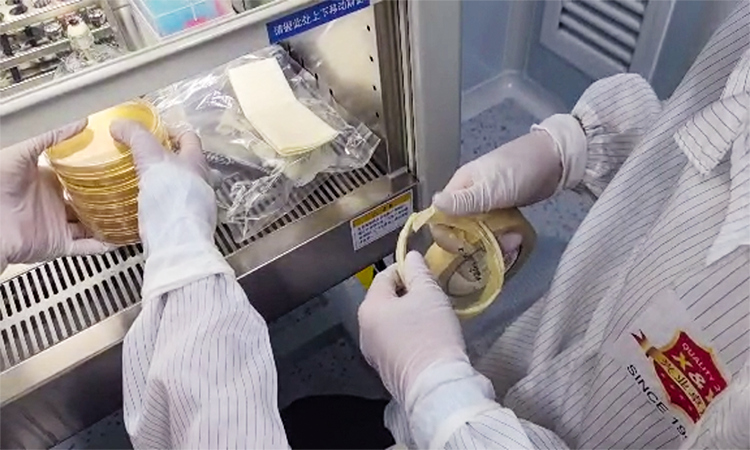
打造優(yōu)質的個人防護產(chǎn)品(pǐn)
在藥品生產和質量控製(zhì)中,微(wēi)生物限度檢查是(shì)一項重(chóng)要的環節。下(xià)麵這篇文章將(jiāng)帶您深入了解詳情。
一(yī)、微生物限度檢查的定(dìng)義和目的
定義:各類產(chǎn)品中檢測和控製微生物汙染的一種方法。
目的(de):確保產品中(zhōng)的(de)微(wēi)生物數量不會對消費者的(de)健(jiàn)康造成潛(qián)在威脅。
二、是否所有非無菌產品均應進行微生物限度檢查?
非無菌產品指的是未經過嚴格滅菌處理的產品,可能會含有一定量的微生物。這些微生物可能來自(zì)原料、生產過程、環境等因(yīn)素。
根據現有的法規和實踐,隻有當產品存在(zài)微生物汙染(rǎn)的風險時,才需要進行微生物限度檢查。

三、微生物限(xiàn)度檢查的方法和(hé)標準
培養法是微生物限度檢(jiǎn)查最(zuì)常(cháng)用的方法之一,其原理是將樣品接種在培養基上,通過培養觀察微(wēi)生物的(de)生長情況,從而確定微生物的數量。
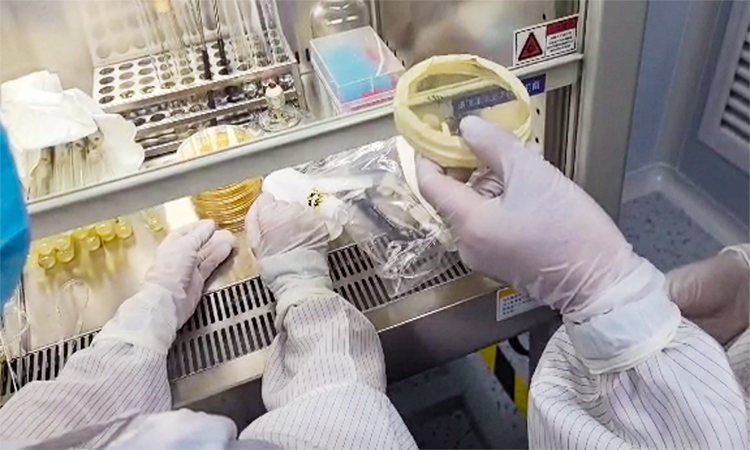
操作方法如(rú)下:
3.1環境要(yào)求(qiú)
1)操(cāo)作(zuò)環境要求極其嚴格,需在特定潔淨度區域內進行;
2)溫度保持在(zài)18-26℃,相對濕度≤65%;
3)全過程必須遵(zūn)守無菌(jun1)操(cāo)作;
4)定期按GB/T 16292-2010、GB/T 16293-2010和GB/T 16294-2010的(de)現行國家標準進行潔淨度驗證。
3.2檢驗量
檢驗量即一次試驗所用的供試品量(g、ml 或cm2);
一般供試品的檢驗量為10g 或10ml;
檢驗(yàn)時,一般應隨機抽取不少於檢驗用量(兩個以上最小包裝單位)的3 倍量供(gòng)試品。

3.3供試液的製備
供試液製備方法要(yào)根據供試品特性,取供試品後將其剪碎,加入緩衝液以200次/min的速率雙麵拍打各3min振搖,作(zuò)為 1∶10 供試(shì)液。
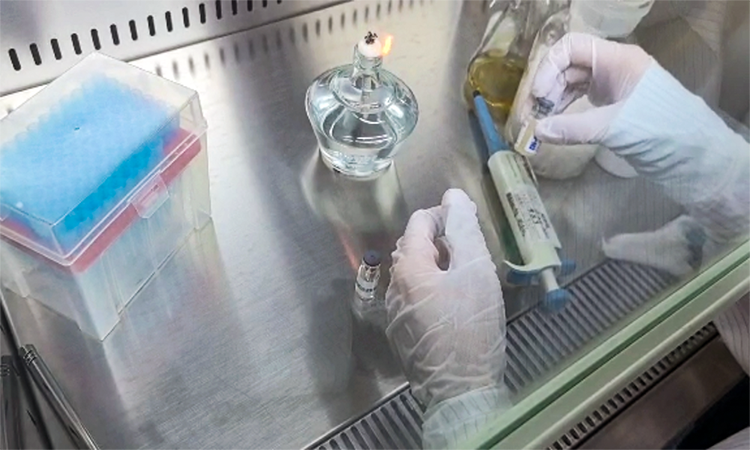
3.4培(péi)養溫度及天數
TSA培養基在生化培養箱中倒置培(péi)養3~5天,30~35℃;SDA培養基在黴菌培養箱中倒置培養5~7天,20~25℃。
每日觀察計算菌落數。
3.5細菌總數計數方法及報告方法
1)菌落蔓延生長成片的平板不宜計數(shù);
2)每張濾膜的菌落數應不超(chāo)過100cfu;
3)以相當於 1g、 1mL 或10cm2供試品的菌(jun1)落數報告菌數;若濾膜上無菌落生長(zhǎng),以小於 1 乘以最低稀釋倍數的值(zhí)報告(gào)菌數。